胃癌
胃癌是什麼?
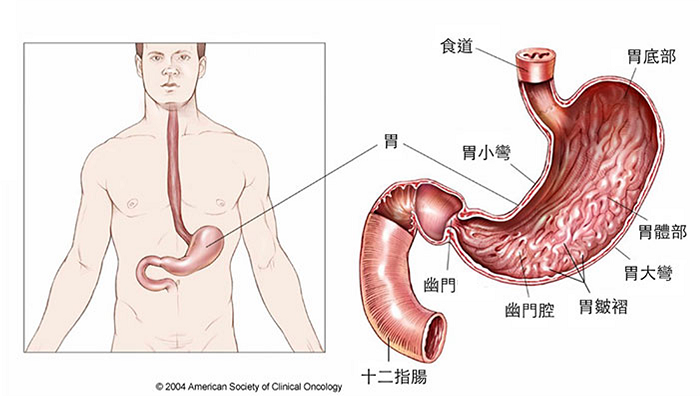
胃癌是從胃部的內壁細胞開始的癌症。胃是位於上腹部的左側的消化食物的器官。胃是消化道的一部分,消化道是一條從口腔到肛門的長而彎曲的管狀中空肌肉器官組成的。消化道負責處理所吃食物中的營養,並幫助將廢物排出體外:
- 食物經由喉嚨通過一條稱之為「食道」的管狀器官進入胃部。
- 食物進入胃部後,會被胃部肌肉將食物和液體與消化液混合,將其分解。
- 離開胃部後,部分被消化的食物會進入小腸,然後進入大腸。
- 大腸的末端稱為「直腸」,它儲存消化食物產生的廢物,直到在排便時從「肛門」排出體外。
胃癌的類型
胃腺癌(adenocarcinoma)開始於胃最內層黏液分泌細胞。幾乎佔最大多數胃癌都是「腺癌」。
根據在胃中形成的部位,胃腺癌可分為兩個主要類別:
- 胃賁門癌開始於胃的最上部約2.5公分處(約一英寸),就是在食道交界處下方的部位。
- 非賁門胃癌是指發生在胃的所有其他部位的癌症。
根據細胞在顯微鏡下的外觀,胃腺癌也可以描述為腸型或瀰漫型:
- 「腸道型腺癌」的分化良好,它在顯微鏡下,癌細胞看起來與正常細胞相似。
- 「瀰漫型腺癌」是未分化或分化較差,意味著在顯微鏡下,癌細胞看起來與正常細胞不同。瀰漫型腺癌的生長和擴散速度比腸道型腺癌更快速,也更難治療。
胃食道交界腺癌(Gastroesophageal junction adenocarcinoma(GEJ))是一種發生在食道與胃賁門交界處的癌症。GEJ的治療方式可能會與胃癌或食道癌類似。
胃腸道神經內分泌腫瘤(Gastrointestinal neuroendocrinetumors,NET)是開始於胃腸道內壁神經內分泌細胞(一種類似神經細胞和荷爾蒙產生細胞的細胞)的癌症。神經內分泌細胞產生的荷爾蒙有助於調節消化液和食物在胃與腸道中移動的肌肉。
胃腸道基質瘤(Gastrointestinal stromal tumors -GIST),它開始於胃壁內及其他消化器官的節律神經細胞。GIST是一種軟組織肉瘤。
原發性胃淋巴瘤,是於胃中形成的一種非何杰金氏淋巴瘤。大多數原發性胃淋巴瘤屬於黏膜相關淋巴組織(MALT)胃淋巴瘤或胃的瀰漫性大型B細胞淋巴瘤(diffuse large B-Cell lymphoma)。
其他罕見的胃癌類型,例如鱗狀細胞癌、小細胞癌和平滑肌惡性肉瘤(leiomyosarcoma),也可能發生於胃部。
現況
根據民國111年(西元2022年)衛生福利部癌症登記報告指出,當年胃癌的發生率排名於男性為第7位、女性為第10位;死亡率的排名於男性為第8位、女性為第7位。
民國111年(西元2022年)初次診斷為胃惡性腫瘤者共計4,377人,占消化器官及腹膜個案數的10.81%;當年死因為胃惡性腫瘤者共計2,277人。
4,377位胃惡性腫瘤個案中,男、女性患者的組織形態分布,均以腺癌最多,分別占男性個案之75.73%,女性個案之67.92%。
資料來源:衛生福利部國民健康署、中華民國111年癌症登記報告。
罹患胃癌的原因與危險因子
胃癌是由於胃細胞的功能發生某些變化而引起的,尤其是當細胞生長和分裂成新細胞的方式時。胃癌的危險因子有很多,但其中許多的危險因子並不直接導致癌症。反之,它們會增加細胞DNA損傷的風險,從而導致罹患胃癌。進一步了解癌症是如何形成的,請參見網站中《什麼是癌症 ?》單元。
危險因子是指任何增加罹患疾病機率的因素。一些胃癌的危險因子,例如吸菸,是可以改變的。然而,危險因子也包括一些人們無法改變的因素,例如年齡和家族病史。了解胃癌的危險因子很重要,因為它能幫助您做出可能預防或降低罹患胃癌風險的選擇。
誰會罹患胃癌
胃癌是全球第五大常見的癌症。胃癌在東亞、西亞、東歐和南美洲的發病率高於美國和其他西方國家。
任何人都有可能罹患胃癌。在美國,黑人、西班牙裔、亞裔或太平洋島民,以及美洲印第安人或阿拉斯加原住民比白人更容易罹患胃癌。男性罹患胃癌的機率幾乎是女性的兩倍,黑人男性死於胃癌的機率也幾乎是白人男性的兩倍。近年來,年輕女性(特別是西班牙裔女性)的胃癌發生率有所上升。胃癌會發生在任何年齡,然而,隨著年齡的增長,罹癌風險也會增加。
胃癌的危險因子
胃癌有多種危險因子。不同的危險因子可能會增加胃部不同部位的癌症風險。例如,幽門螺旋桿菌(H. pylori)感染會增加胃下部和中部的罹癌風險,而肥胖與胃食道逆流症(GERD)則是會增加胃上部罹癌的風險。
ㄧ、感染幽門螺旋桿菌(H. pylori infection)
胃黏膜層的慢性幽門螺旋桿菌感染是導致胃癌的一個主要危險因子。這種細菌透過與唾液、嘔吐物或糞便的直接接觸在人與人之間傳播。雖然許多慢性幽門螺旋桿菌感染者沒有症狀,但有些人會變成胃潰瘍或胃部發炎(一種稱為萎縮性胃炎)。對某些人而言,萎縮性胃炎會導致胃黏膜病變越來越嚴重,最終發展成胃癌或胃粘膜相關的淋巴組織(MALT)之淋巴瘤。治療幽門螺旋桿菌感染可降低這些類型的胃癌風險。
二、其他的醫療狀況
以下的人群會增加罹患胃癌的風險:
- 慢性萎縮性胃炎(因為長期胃部發炎導致胃腺體細胞變薄)
- 伴隨著腸上皮化生的萎縮性胃炎(原本正常的胃黏膜細胞因慢性發炎被腸道內壁出現的細胞所取代)
- 感染Epstein-Barr (EB)病毒
- 惡性貧血(一種自體免疫性疾病,腸道無法正常吸收維生素B12,導致紅血球體積增大且數目過低)
- 肥胖(體重過重)
- 胃食道逆流疾病(胃酸反覆逆流至食道的情形)
三、遺傳與家族病史
有下列情況的人,罹患胃癌風險會增加,有時甚至會非常高:
- 有一位直系親屬(父母、兄弟姊妹或子女)罹患胃癌
- 家族性癌症症候群,例如:
- 家族性腺瘤性息肉病
- 家族性腸型胃癌(familial adenomatous polyposis,FIGC),它是一種家族內會發生的遺傳性疾病,但沒有已知基因原因的胃癌
- 胃腺癌與胃近端多發息肉症(Gastricadenocarcinoma and proximal polyposis of thestomach-GAPPS)
- 遺傳性瀰漫型胃癌(Hereditary diffuse gastriccancer-HDGC)
- 少年型息肉群(Juvenile polyposis syndrome)
- 李-佛美尼(Li-Fraumeni)症侯群
- 林奇(Lynch)症候群(又稱遺傳性非息肉性大腸癌,Hereditary nonpolyposis colon cancer-HNPCC)
- 黑斑息肉(Peutz-Jeghers) 症侯群
- 血型A型
四、飲食
飲食中水果與蔬菜量攝取少,或攝取高鹽、高煙燻、保存不良的食物,這些都可能增加罹患胃癌的風險。
五、吸菸
吸菸者罹患胃癌風險高於不吸菸者,吸菸也會降低幽門螺旋桿菌感染的治療效果,戒菸者罹患胃癌的風險會隨著時間的推移而降低。
延伸閱讀:「 戒菸的理由與如何戒菸 」。
六、暴露在某些環境與職業
下列人群會增加罹患胃癌的風險:
- 在橡膠或煤炭產業工作的人
- 暴露於非常高劑量輻射下的人
有一個或多個以上這些危險因子,並不意味著您一定會罹患胃癌。許多有危險因子的人卻從未罹患胃癌,而一些沒有已知危險因子的人則罹患了胃癌。如果您認為自己可能屬於高風險,請諮詢您的醫師。
具有特定基因疾病或家族病史等高風險人群,可能可以接受胃癌篩檢或預防性手術。
延伸閱讀,認識「 胃癌篩檢 」。
胃癌的症狀
早期胃癌通常沒有症狀,因此難以發現。症狀通常在癌症擴散後才開始出現。
早期胃癌發生的可能症狀,包括:
- 消化不良和胃部不適
- 飯後飽脹感
- 輕微噁心
- 食慾減退
- 胃灼熱感
晚期胃癌(癌症已經轉移/擴散到胃部以外的身體其他部位)的症狀,早期胃癌的症狀可能包括:
- 糞便中有血
- 嘔吐
- 不明原因的體重減輕
- 胃痛
- 黃疸(眼睛鞏膜(眼白)和皮膚發黃)
- 腹水(腹部積液)
- 吞嚥困難
這些症狀可能由胃癌以外的其他疾病引起,若您有這些症狀,請務必詢問您的醫師。醫師會詢問您何時的出現症狀以及症狀發作的頻率。如果是胃癌,若您忽略這些症狀可能會延誤治療,並且會降低治療的效果。
診斷胃癌
如果您有胃癌的症狀,醫師需要確定這些症狀是否由癌症或其他疾病引起。醫師可能會:
- 詢問您的個人與家族病史,以了解您是否有罹患胃癌的危險因子
- 進行身體檢查,包括觸診您的腹部是否有異常
- 進行血液檢查,檢查是否有貧血(紅血球數目低),這可能是胃部出血的跡象
- 檢查糞便中是否有潛血(隱藏的血液),這可能也是胃部出血的跡象
根據這些檢查結果,醫師可能會建議您進一步檢查,以確定是否罹患胃癌。
診斷胃癌的檢查
以下檢查和程序是用於診斷胃癌,這些檢查的結果也能幫助您與醫師共同擬定治療計畫。
上消化道內視鏡切片檢查
上消化道內視鏡是檢查食道、胃和十二指腸(小腸的第一部分)內是否有異常部分的檢查。內視鏡是一條細長、帶有光源的管子,經由口腔進入喉嚨,接著進入食道。內視鏡還配有一個切除細胞或組織檢體(切片)的工具,切下的組織會交由病理醫師在顯微鏡下檢查是否有癌變跡象。
請詢問您的醫師,了解在做切片時與切片後應注意哪些事項。
若想了解病理報告中包含哪些資訊,可以前往「 病理報告 」單元查閱。
鋇劑造影(Barium swallow)
鋇劑造影是針對食道和胃的一種特殊X光檢查。病人會喝下一種含有鋇(一種銀白色金屬化合物)的顯影劑,鋇液會包覆食道和胃部,然後進行X光照攝,此程序又稱為上消化道X光攝影(upper GIseries)檢查。
電腦斷層掃描
電腦斷層掃描(CT scan)將X光機連結到電腦,從不同角度拍攝體內多張詳細的影像。為了讓器官或組織更清楚的顯影出來,可能會注射或口服顯影劑。此檢查也稱為「電腦斷層攝影」。
生物標記檢測
「生物標記」檢測是一種尋找基因、蛋白質和其他物質(稱為生物標記或腫瘤標記),這些物質可以提供有關癌症的資訊。有些生物標記會影響某些癌症治療的效果,生物標記檢測可能有助於您和醫
師決定最適合您的治療方式。
為了檢測這些生物標記,需要在切片或手術時取得胃癌組織檢體。這些檢體會送到實驗室檢測,以確認胃癌細胞是否具有這些生物標記。
胃癌的生物標記檢測,包括下列:
- 第二型人類上皮細胞生長因子(HER2):癌細胞中的HER2蛋白可能高於正常細胞的HER2蛋白。
- PD-L1:這些細胞表面可能含有較高量的免疫檢查點蛋白,也稱為PD-L1。
- 微衛星不穩定(Microsatellite instability):細胞可能存在微衛星不穩定性,這可能是由於DNA複製過程中的錯誤無法修正。
- 錯配修復缺失(Mismatch repair deficiency):細胞可能有錯配修復基因缺陷。
- 腫瘤突變負荷(Tumor mutational burden):細胞的腫瘤突變負荷量高,則表示有許多基因突變。
- 神經營養因子受體酪氨酸激酶(NTRK) :細胞可能有NTRK基因的變化。
延伸閱讀,請參見網站「 癌症治療的生物標記檢測 」單元。
胃癌分期的檢測
若您診斷為胃癌,您將轉診給腸胃道腫瘤科醫師,他是專門診斷和治療胃腸道腫瘤的醫師。醫師會建議您進行一些檢查,以確定癌症是否已轉移或擴散,如果已轉移或擴散,那已經到什麼樣的程度。有時癌症僅局限在胃部,有時則已轉移或擴散至身體其他部位。了解癌症在體內擴散程的過程稱為「分期」,了解胃癌的分期資訊對於制定治療計畫非常重要。以下影像檢查和程序可能用於確定您的胃癌期別:
- 內視鏡超音波檢查是將內視鏡經口腔或直腸插入體內。內視鏡是一條細長的帶有光源的管子,末端有超音波探頭,用於將高能量聲波(超音波)偵測內部組織或器官並產生迴聲,形成組織的影像,此程序也稱「超音波內視鏡鏡檢」。
- PET-CT掃描是結合正子斷層掃描(PET)與電腦斷層掃描(CT)所取得的影像。PET與CT掃描是在同一台機器同時進行,兩種掃描的影像合併,會產生比單獨進行的任一檢查更詳細的影像。
- PET掃描時,會將少量「放射性葡萄糖」注入靜脈。掃描儀圍繞身體旋轉,拍攝體內葡萄糖吸收的影像,癌細胞在影像中會顯示得更亮,是因為它們比正常細胞更活躍,吸收更多葡萄糖。
- CT掃描是從不同角度拍攝一系列詳細的X光影像,會注射或口服顯影劑,幫助器官或組織的更清楚的顯影出來。
- 磁振造影(MRI)加含釓顯影劑:是一種利用磁力、無線電波和電腦,取得體內詳細影像。靜脈注含釓顯影劑後,顯影劑會集中在癌細胞周圍,使得癌細胞在影像中顯影更清晰,此程序又稱為核磁共振成像。
- 腹腔鏡檢查是一種外科手術,用於檢查腹腔內的器官是否有疾病的徵兆。手術會在腹部切開幾個小切口,然後將腹腔鏡(一根細長、帶光源的管子)插入其中一個切口,其他器械,也可透過相同或其他切口處插入,進行摘除器官或採集組織檢體,會將檢體送至實驗室檢查是否有癌症。手術中也可能以溶液沖洗腹腔然後取出細胞,再將細胞放到顯微鏡下觀察,確認是否有癌細胞。
有些人會選擇尋求第二意見
您可能會想尋求第二意見以確認您的胃癌診斷與治療計畫。若要尋求第二意見,您需要取得您於第一位醫師所做的檢查結果和報告,並交給第二位醫師參考。在第二位醫師提供他的意見前,他會檢視病理報告、切片及影像。給予第二意見的醫師,他可能會同意第一位醫師的診斷與治療計畫,也可能提出修改意見或其他做法,或提供更多有關您的癌症訊息。
:
華人癌症資訊網也提供線上詢問第二意見,請前往網站首頁“ 我要發問 ”,或您可前往其他醫院尋找合適的醫師聽取第二意見。關於就診時可能想詢問一些問題,您可以於網站中「向醫師詢問有關癌症的問題 」中取得相關資訊。
胃癌分期
癌症的分期是描述癌症在體內的擴散程度,例如腫瘤的大小、是否已經擴散,以及離最初形成處擴散的多遠。知道胃癌的分期對於制定最佳治療方案非常重要。
有多種癌症的分期系統用於描述癌症的擴散程度,胃癌通常是採用TNM分期系統,您的病理報告中會使用這套分期系統描述癌症的狀況。根據TNM的結果,癌症劃分為某個期別(I、II、III 或 IV,也寫作1、2、3 或4)。當醫師在與您討論您的狀況時,會用這些期別來描述癌症狀況。
以下資訊是關於胃腺癌的分期,這是最常見的胃癌類型。
胃壁的結構
胃壁由五層組織與肌肉組成,了解這些層有助於您了解癌症的分期:
- 黏膜層(mucosa)是胃壁的最內層,它是由上皮細胞和腺體細胞組成。腺體細胞分泌黏液來保護胃壁,以及分泌消化液協助幫助分解食物。大部分胃癌都從黏膜層的腺體細胞開始,起源於腺體細胞的癌症稱之為腺癌。
- 黏膜下層(submucosa)位於黏膜層和肌肉層之間的結締組織層,它包含血管、淋巴管和神經細胞。
- 肌肉層(muscle layer)位於黏膜下層的下一層,肌肉層幫助胃將食物與消化液混合,及將食物推送到小腸以利營養吸收。
- 漿膜下層(subserosa)位於肌肉層與漿膜層之間的一層薄薄的結締組織層。
- 漿膜層(serosa)是胃壁的最外層。
胃癌隨著從黏膜層逐步擴散到外層,其病情也跟著越發嚴重。
第0期(原位癌)胃癌
第0期也稱為原位癌,指的是在胃的黏膜層中發現異常細胞。這些異
常細胞可能會變成為癌症,並擴散至附近正常的組織。
第I期(第1期)胃癌
第I期胃癌可細分為IA期和IB期。
- IA期,
- 癌症已在黏膜層形成,並可能已擴散到黏膜下層(T1),但沒有淋巴結侵犯(N0)。
- IB期,
- 癌症已在黏膜層形成,並可能已侵入至黏膜下層(T1),且已轉移到附近1或2個淋巴結內(N1);或
- 癌症已從黏膜層侵入至肌肉層(T2 N0)。
關於第I期胃癌的治療,請見依期別治療單元。
第II期(第2期)胃癌
第II期胃癌可細分為IIA期和IIB期。
- IIA期,
- 癌症可能已侵入至黏膜下層(T1),並已轉移到附近3到6個淋巴結內(N2);或
- 癌症已侵入至肌肉層(T2)及轉移到附近1或2個淋巴結內(N1);或
- 癌症已侵入至漿膜下層(T3 N0)。
- IIB期,
- 癌症可能已侵入至黏膜下層(T1),並轉移到附近7到 15個淋巴結內(N3a);或
- 已侵入至肌肉層(T2)並轉移到附近3到6個淋巴結內(N2);或
- 已侵入至漿膜下層(T3)及轉移到附近1或2個淋巴結(N1);或
- 已侵入至漿膜層(T4a N0)。
關於第II期胃癌的治療,請見依期別治療單元。
第III期(第3期)胃癌
第III期胃癌可細分為IIIA、IIIB和IIIC。
- IIIA期,
- 癌症已侵入至肌肉層及轉移至附近7到15個淋巴結內(T2 N3a);或
- 癌症已侵入至漿膜下層及轉移至附近3到6個淋巴結內(T3 N2);或
- 癌症已侵入至漿膜層及轉移至附近1到6個淋巴結內(T4a N1-2);或
- 癌症已侵入至鄰近器官,例如:脾臟、大腸、肝臟、橫膈膜、胰臟、腹壁、腎上腺、腎臟或小腸,或後腹腔。
- IIIB期,
- 癌症可能已侵入至黏膜下層或肌肉層,並已經轉移至附近16個以上的淋巴結內(T1-2 N3b);或
- 癌症已侵入至漿膜下層或漿膜層,並癌症已經轉移至附近7到15個淋巴結內(T3-4a N3a);或
- 癌症已侵入至鄰近器官,例如:脾臟、大腸、肝臟、橫膈膜、胰臟、腹壁、腎上腺、腎臟或小腸,或後腹腔,並癌症已經轉移至附近1到6個淋巴結內(T4b N1-2)。
- IIIC期
- 癌症已侵入至漿膜下層或漿膜層,並已經轉移至附近16個或16個以上的淋巴結(T3-4a N3b);或
- 癌症已侵入至鄰近器官,例如:脾臟、大腸、肝臟、橫膈膜、胰臟、腹壁、腎上腺、腎臟或小腸,或後腹腔,並癌症已經轉移至附近7個或7個以上的淋巴結內(T4b N3a-3b)。
關於第III期胃癌的治療,請見依期別治療單元。
第IV期(第4期)胃癌
IV期,癌症已遠端轉移至其他部位(M1),如:肺、肝臟、遠端淋巴結和腹膜等。
第 IV 期胃癌又稱為轉移性胃癌。當癌細胞透過淋巴系統或血液轉移,並在身體其他部位形成腫瘤,這就稱為轉移性癌症。轉移性腫瘤與原發性腫瘤同屬相同的癌症。例如,若胃癌轉移到肺部,肺部的癌細胞其實就是胃癌細胞,這時稱為「轉移性胃癌」,而非肺癌。
進一步學習,請閱讀網站「 轉移性癌症:當癌症擴散時 」單元。
關於第IV期胃癌的治療,請見依期別治療單元。
胃癌的復發
胃癌的復發是指治療後癌症再次發生。癌症的復發可能會在胃部、
淋巴結或身體其他部位,如肝臟、肺或骨骼。會進行檢查以判斷癌症復發的位置,胃癌的復發其治療方式將取決於復發的部位。
想進一步瞭解,請參考「 癌症的復發:當癌症再回來 」。
有關如何應對與醫療團隊溝通的建議,請參考「胃癌的應對」。
關於胃癌復發的治療,請見治療單元。
治療胃癌
胃癌有多種治療方式可供選擇。您和您的癌症照護團隊將共同決定治療計畫,該計劃可能包括一種以上的治療方法。會考量許多因素,例如癌症的期別、您的整體身體狀況以及您個人的意願。治療計畫將包含您的癌症各項數據、治療目標、治療選項及可能的副作用,以及預期治療的時間。
在治療開始前與癌症照護團隊溝通預期可能會出現的情況,這對病人和家屬會有所幫助。了解在治療前需要做些什麼、治療期間可能有的感受,以及所需的協助。延伸閱讀,請前往網站《 向醫師詢問治療問題 》單元。
ㄧ、內視鏡黏膜切除術(Endoscopic mucosal resection,簡稱EMR)
內視鏡黏膜切除術是一種使用內視鏡切除消化道內壁原位癌及早期癌症的治療方法。內視鏡是一根細長的管狀儀器,配有光源、鏡頭以及用於切除組織的工具。
二、外科手術治療
外科手術是胃癌常見的治療方式。手術的類型取決於癌症發生的部位。
除了外科手術之外,還會有其他的治療:
- 手術前進行的治療稱為「術前」治療或「新輔助」治療。手術前可能會給予化學治療,以縮小腫瘤,並減少手術中需要切除的組織量。目前正在「研究」術前進行同步化放療以縮小腫瘤。
- 手術後為了降低癌症的復發風險而進行的治療稱為「輔助治療」。醫師切除所有可見腫瘤後,第二、三期病人可能會在接受化學治療,以殺死殘留的癌細胞。
胃切除手術 (Gastrectomy)
胃切除手術是切除部分或全胃,是胃癌的治療主要方式,包括:
- 次全胃切除手術(Subtotal gastrectomy):指的是切除胃部癌細胞的部位、附近的淋巴結以及腫瘤附近的其他組織和器官,可能也同時切除脾臟。
- 全胃切除手術(Total gastrectomy):指的是切除整個胃部、附近的淋巴結以及食道、小腸和腫瘤附近組織的其他組織,脾臟也可能會切除。手術後,醫師會將食道連結到小腸,以便病人能夠繼續進食和吞嚥。
三、腔內支架置放術(Endoluminal stent placement)- 緩解阻塞症狀
當腫瘤「阻塞」進出胃部的通道時,可能會進行腔內支架置放術。該手術中,醫師會從食道到胃或從胃到小腸放置一根支架(一根細長、可擴張的管子),以便讓病人能夠正常進食。
四、內視鏡雷射治療(Endoluminal laser therapy)- 緩解阻塞症狀
內視鏡雷射治療是一種使用內視鏡(一根細的、但有光源的管子),連接雷射作為手術刀來打開腸胃道「阻塞」部位的治療方式。
五、胃空腸繞道手術 (Gastrojejunostomy) - 緩解阻塞症狀
胃空腸繞道手術是切除因癌症「阻塞」小腸開口的胃癌部位,然後,外科醫師將胃與空腸(小腸的一部分)連接起來,以便讓食物和藥物能順利從胃部進入小腸。
六、放射治療
放射治療利用高能量X光或其他類型的放射線殺死或抑制癌細胞的生長。極少數胃癌會採用體外放射治療,即使用體外的放射線機器直接照射到體內的腫瘤部位進行治療。
延伸閱讀,認識「體外放射治療」和「 放射治療的副作用 」。
七、化學治療
化學治療(簡稱「化療」)是使用藥物來抑制癌細胞生長,透過殺死癌細胞或阻止癌細胞分裂來達成效果。
胃癌的化學治療通常是全身性治療,指的是口服藥物或將藥物注射到靜脈,進入血液到達全身的癌細胞。
治療胃癌的化療藥物包括(依字首英文字母排序):
- Capecitabine (商品名: Xeloda 截瘤達錠)
- Cisplatin
- Docetaxel (商品名: Taxotere 剋癌易注射劑)
- Doxorubicin (俗稱小紅莓)
- Epirubicin
- 氟尿嘧啶(5-FU)
- Irinotecan (商品名: Campto 抗癌妥)
- Leucovorin
- Oxaliplatin
- Paclitaxel
- Trifluridine and tipiracil
延伸閱讀,了解有關化療的作用原理、給藥方法、常見副作用等更多資訊,請前往網站中「 化療治療 」查閱。
標靶治療是使用藥物或其他物質來攻擊特定癌細胞。醫師可能會建議做生物標記檢測,以幫助預測對特定標靶治療藥物的反應。
延伸閱讀,認識「 癌症治療的生物檢測 」。
治療胃癌常用的標靶治療藥物,包括:
- Ramucirumab (商品名:欣鋭擇)
- Regorafenib (商品名:癌瑞格)
- Trastuzumab (商品名:賀癌平)
- Trastuzumab deruxtecan (商品名:優赫得)
- Zolbetuximab (商品名:威絡益)
延伸閱讀《 標靶治療與癌症 》。
九、免疫治療
免疫治療幫助人體的免疫系統對抗癌症。醫師可能會建議您做生物標記檢測,以幫助您預測特定免疫治療藥物的反應。延伸閱讀,認識「 癌症治療的生物檢測 」。
胃癌常用的免疫治療藥物,包括:
- nivolumab(商品名Opdivo,中文名保疾伏)
- pembrolizumab(商品名Keytruda,中文名吉舒達)
這些藥物透過多種途徑殺死癌細胞,它們也被視為標靶治療,因為它們會針對癌細胞中的特定變化或物質發揮作用。
延伸閱讀《 免疫治療與癌症 》以及《 免疫治療的副作用 》。
腹腔溫熱化學治療(Hyperthermic intraperitonealchemotherapy - HIPEC)- 仍探索研究用
局部化學治療是將化療藥物直接注射到器官或體腔,如腹腔中,主要是攻擊該區域的癌細胞。
腹腔溫熱化學治療也稱熱化學治療)是一種局部化療方式,目前正「研究」用於胃癌治療,僅部分醫學中心有使用此治療的經驗。外科醫師會先盡可能切除癌症組織,再將經加熱的化療藥物(如mitomycin或cisplatin)經由導管注入腹腔,持續約2小時。之後,醫師會將化療藥物從腹部引流排出,並在縫合切口前沖洗腹腔。
治療性的臨床試驗,目的在幫助改進現有治療或獲取癌症病人新治療資訊的研究。對某些病人而言,加入臨床試驗可能是一種治療的選項。
欲了解更多進行中的臨床試驗您可以從「 台灣臨床試驗資訊平台」、各醫院臨床試驗中心的網站查詢、詢問您的主治醫師。
延伸閱讀,請前往網站《 認識試驗資訊 》單元,閱讀更多關於臨床試驗相關資訊。
十二、後續追蹤檢查
為了觀察治療效果,一些用於診斷或分期的檢查可能會重複進行。根據這些檢查的結果,決定治療是否繼續、改變或停止。這些檢查有時稱為追蹤檢查或定期檢查。
您也可能需要做腫瘤標記檢查,例如CEA與CA 19-9的血液檢查。這些標記的數值升高可能表示胃癌復發。
胃癌依照期別治療
癌症分期是決定胃癌最佳治療方案的重要因素,其他因素,例如您的偏好與整體身體狀況,也同樣重要。
對某些人來說,加入臨床試驗可能是一種治療的選項,可詢問您的主治醫師是否有新的抗癌藥物或治療組合的臨床試驗能參加。若想了解更多有關臨床試驗的資訊,包括如何找到與參加試驗,請前往網站「 臨床試驗資訊 」單元。
胃癌第0期(原位癌)的治療
第0期(原位癌)胃癌的主要治療方式是胃切除手術(手術切除全部或部份的胃以及附近的淋巴結)。
內視鏡黏膜切除術是使用內視鏡切除消化道內壁的異常生長物或組織或病變,無需開腹手術。此手術適用於腫瘤較小且有較小風險轉移到附近淋巴結的人。
了解更多有關治療方式的資訊,請參見前面「治療胃癌」單元。
胃癌第I期的治療
第I期胃癌的主要治療方式是胃切除手術(手術切除全部或部份的胃以及附近的淋巴結)。部分病人可能會在手術之前或之後接受化學治療。
治療第I期胃癌常用的化學治療藥物包括:
capecitabine、cisplatin、docetaxel、epirubicin、fluorouracil(5-FU)、leucovorin與oxaliplatin,這些化學治療藥物可單獨使用或合併使用。
對於腫瘤小、轉移風險低的人,內視鏡黏膜切除術可能是一種侵入性較小的選擇。
想了解更多有關這些治療方式的資訊,請參見前面「胃癌治療」單元。|
胃癌第II期與第III期的治療
治療第II期與第III期胃癌的主要治療方式胃切除手術(手術切除全部或部份的胃及附近的淋巴結)。部分病人可能會在手術前或手術後接受化學治療和/或合併免疫治療。
治療第II期與第III期胃癌的化學治療藥物包括:
capecitabine、cisplatin、docetaxel、epirubicin、fluorouracil (5-FU)、leucovorin和oxaliplatin,這些藥物可單獨使用或合併使用。
想了解更多有關這些治療方式的資訊,請參見前面「胃癌治療」。
治療第IV期胃癌、無法手術切除的胃癌及胃癌復發
對於第IV期胃癌、任何分期但無法手術切除的胃癌以及胃癌的復發治療,都屬於緩和治療,緩和治療的目的是改善嚴重或威脅生命的疾病(如癌症)病人的生活品質。許多相同的癌症的治療方式,如化學治療、其他藥物和放射治療,也能作為緩和治療,以幫助病人感到更舒適。
若想進一步認識緩和療法,請參見網站中「 緩和照護 」單元。
HER2陰性腫瘤的第一線緩治療可能包括:化學治療加上或沒有加上免疫治療藥物nivolumab或化學治療加上標靶藥物zolbetuximab。
對於HER2陽性腫瘤,可能包括免疫治療藥物pembrolizumab與標靶藥物trastuzumab合併化學治療。後續的緩和治療可能包括:
- 化學治療
- 單用ramucirumab(商品名:欣鋭擇)或合併化療一起使用
- Pembrolizumab(商品名:吉舒達),適用於DNA錯配修復缺失、高度微衛星不穩定或高度腫瘤突變負荷的癌症
- Trastuzumab deruxtecan(商品名:優赫得),適用於HER2陽性癌症
許多化學藥物可用在晚期胃癌的緩和治療,包括:
capecitabine、cisplatin、docetaxel、doxorubicin、epirubicin、etoposide、fluorouracil(5-FU)、irinotecan、leucovorin、oxaliplatin、paclitaxel 和 trifluridine 和 tipiracil,這些藥物可單獨或合併使用。
如果您因癌症或其治療而出現副作用,醫療團隊可能會給予其他治療,幫助您減輕副作用,讓您感到更舒適。例如:如果您胃阻塞,可能接受腔內雷射治療、腔內支架置放術或胃空腸繞道手術來解決阻塞問題。放射治療或手術也可能用來止血、減輕疼痛或縮小阻塞胃的腫瘤。
想了解更多這些治療方式的資訊,請參見前一「胃癌治療」單元。
與胃癌共處
胃癌與其治療可能會帶來生理與心理上的副作用。當您剛知道自己罹患胃癌時,可能會擔心如何面對接下來的變化。您可以採取的一個步驟是多了解可能會發生的變畫,以及有哪些資源是能幫助您。說出您想知道的任何問題與擔憂時,會讓您感到更有掌控感。您的醫療團隊也會和您討論如何減輕副作用,讓您減輕擔憂。
想了解胃癌治療常見的身體副作用,請參見本文「胃癌治療」章節,想進一步了解治療癌症的副作用處理,您可以前往網站中「癌症治療的副作用處理」單元。如需了解如何網站中面對心理副作用,請參見「情緒與癌症」單元。
飲食與營養的變化
胃癌及其治療可能會影響您進食足夠的食物或吸收食物中營養的能力。若您的胃部分或全部切除,則您可能需少量地進食、增加進食次數,或調整飲食內容。醫師或營養師可能會建議您在用餐後保持直立一段時間,並協助您調整飲食,以確保您能獲得足夠的營養。
如需更多關於癌症治療期間的飲食建議,請參見「 營養照顧 」單元。
身體形象的改變
胃癌與其治療可能會改變您的外貌與自我感受。請記得,您不是唯一有這種感覺得人,學習適應身體形象與自我認同的改變需要一些時間,但許多人在此過程中慢慢學會調適心態並繼續前進。
想進一步了解癌症治療如何影響自我形象與性生活,以及調適與表達您的感受,請參見網站中「癌症如何影響自我形象與性」。
面對追蹤檢查的壓力
許多接受胃癌治療的人需要定期回診,接受追蹤檢查或檢測。安排與規劃這些事情可能讓人感到壓力與花時間,而等待檢查結果的這段時間會讓人趕到焦慮,並擔心癌症是否會復發。醫療費用,如掛號費、自費藥品、停車費與交通費等等,也都會帶來更多的壓力。
想了解如何面對癌症復發的恐懼,請閱讀網站中「治療後的生活」單元。
資料來源:
“Coping with Stomach Cancer was originally published by the National Cancer
Institute.”
臺大醫院腫瘤醫學部部主任 葉坤輝教授 協助校稿
更新日期:2025.07.03


